

近日,甘李药业在研胰岛素产品甘精U300在中国完成的一项I期临床研究成果在国际权威学术期刊《Frontiers in Endocrinology》上成功发表。该论文表明,甘李甘精胰岛素在健康受试者中与原研参照药在安全性、药代动力学及药效动力学方面具有生物相似性。《Frontiers in Endocrinology》作为一份全球性的内分泌代谢领域权威学术期刊,其2023年最新影响因子为3.9,引用量188,000,中科院分区二区,在业界具有广泛的影响力。

图1-文章发表页面截图
(图片来源:《Frontiers in Endocrinology》)
甘精胰岛素U300(以下简称“甘精U300”)是一款基于甘精胰岛素U100改良的长效基础胰岛素,相较于甘精胰岛素U100,甘精U300的作用时间更长,日间变异度更低,低血糖风险更低1。在国内,甘精U300目前仅有赛诺菲的来优时®️上市。甘李药业在研的甘精U300是来优时®️的生物类似药。根据国家法规要求,生物类似药的上市许可需证明其在质量、安全性和有效性方面与已获批准的原研参照药具有高度相似性2。人体正葡萄糖钳夹技术是公认最合适评价胰岛素制剂间相似性的方法,故胰岛素生物类似药的临床研究应首先开展钳夹试验比对候选生物类似药与原研参照药间药代动力学(PK)和药效动力学(PD)的生物等效性3。
因此,甘李药业在中国开展了一项随机、双盲、单中心、I期正葡萄钳夹临床试验,在健康受试者中评估了甘李甘精U300与原研参照药来优时®️在安全性,PK和PD方面是否具有生物等效性。本研究主要PK终点为甘精代谢物M1 0-24小时的曲线下面积(AUC0-24h)和给药后24小时内甘精最大浓度(Cmax)。主要PD终点为0到24小时葡萄糖输注速率(GIR)曲线下面积(AUCGIR0-24h)和给药后24小时内最大GIR (GIRmax)。
文章指出,在PK和PD方面,甘李甘精U300显示出与来优时®️相当的PK参数和PD反应,90%的置信区间在80%至125%等效值边界之内。在安全性方面,甘李甘精U300与来优时®️无显著性差异(图2)。研究结果显示,甘李甘精胰岛素U300在健康受试者中被证明与原研参照药来优时®️在安全性,PK及PD方面具有生物等效性。
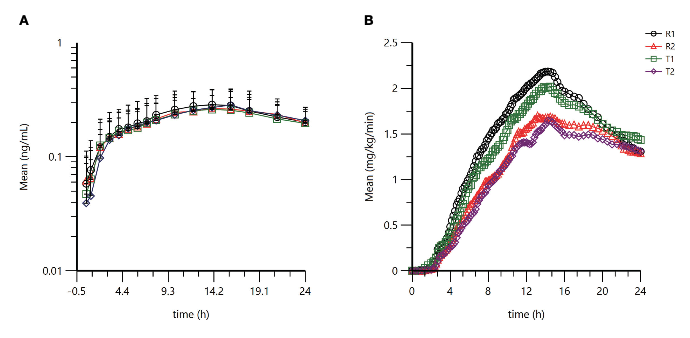
图2 药代动力学和药效动力学结果
(A)皮下注射试验产品T或参比产品R后M1的半对数平均血药浓度-时间曲线
(B)皮下注射试验产品T或参比产品R后的平均GIR-时间曲线
甘李药业CEO都凯表示:“本次在健康受试者中开展的I期临床研究证明了甘精U300与原研参照药来优时®️具有生物相似性,为甘李甘精U300作为生物类似药提供了真实可靠的依据。甘精U300作为甘李药业甘精胰岛素(长秀霖®️)系列的新一产品,其临床研究的积极结果进一步验证了甘李甘精胰岛素质量的可靠性。我们将积极推动该产品早日上市,为糖尿病患者带来更多质优价宜的用药选择。”
论文链接:
https://www.frontiersin.org/journals/endocrinology/articles/10.3389/fendo.2024.1407829/full
参考文献:
1. Joshi SR, Singh G, Marwah A, Mittra S, Suvarna VR, Athalye SN. Comparative clinical efficacy and safety of insulin glargine 300 U/ml (Toujeo) versus insulin glargine 100 U/ml in type 2 diabetes and type 1 diabetes: A systematic literature review and meta-analysis. Diabetes Obes Metab. (2023). doi: 10.1111/dom.15007
2. SONG Li-na, XU Gang-ling, GE Yu-mei, TANG Chong-qi, XIE Song-mei. Quality Similarity Evaluation and Technical Requirement of Biosimilar Products[J]. Chinese Pharmaceutical Journal, 2022, 57(23): 1954-1961 https://doi.org/10.11669/cpj.2022.23.001
3. 国家药监局药审中心.《胰岛素类产品生物类似药药学研究与评价技术指导原则》的通告(2022年第22号)。2022.03.10
关于甘李药业
甘李药业股份有限公司(简称:甘李药业,股票代码:603087.SH)作为中国第一家掌握产业化生产重组胰岛素类似物技术的高科技生物制药企业,具备完整胰岛素研发管线。
目前,公司拥有六款核心胰岛素产品,包括五个胰岛素类似物品种:长效甘精胰岛素注射液(长秀霖®)、速效赖脯胰岛素注射液(速秀霖®)、门冬胰岛素注射液(锐秀霖®)、预混精蛋白锌重组赖脯胰岛素混合注射液(25R)(速秀霖®25)、门冬胰岛素30注射液(锐秀霖®30);以及人胰岛素品种:预混精蛋白人胰岛素混合注射液(30R)(普秀霖®30),产品覆盖长效、速效、预混三个胰岛素功能细分市场。同时,公司产品覆盖相关医疗器械,包括可重复使用的胰岛素注射笔(秀霖笔®)和一次性注射笔用针头(秀霖针®)。
在 2024 年中国胰岛素接续采购中,甘李药业的胰岛素类似物采购需求在所有中选企业中排名第二,在国内企业中排名第一。公司的国际化进程也在不断推进,一次性注射笔用针头(秀霖针®)在2020年获得美国食品药品管理局(FDA)批准。同时,2024年公司通过了欧洲药品管理局(EMA)的 GMP 检查。这标志着公司在国际和国内市场上的竞争力得到大幅提升。
未来,甘李将努力实现糖尿病治疗领域的全面覆盖,进一步提升公司在糖尿病治疗领域的市场竞争力。公司还将积极开发新的化学药和生物新药,重点关注代谢性疾病、心血管疾病和其他治疗领域。